Ladda litiumbatteri
Metod 1. Labaggregat + lite teori
"Lithium Ion Charging Profile"
OBS viktigt. Se specifikt batteris datablad vad som gäller med strömmar och spänningar. Nedan en allmän sammanfattning. Nedan en typiskt laddnings -karaktäristik för ett litiumbatteri. Denna sida handlar om att förstå denna kurva.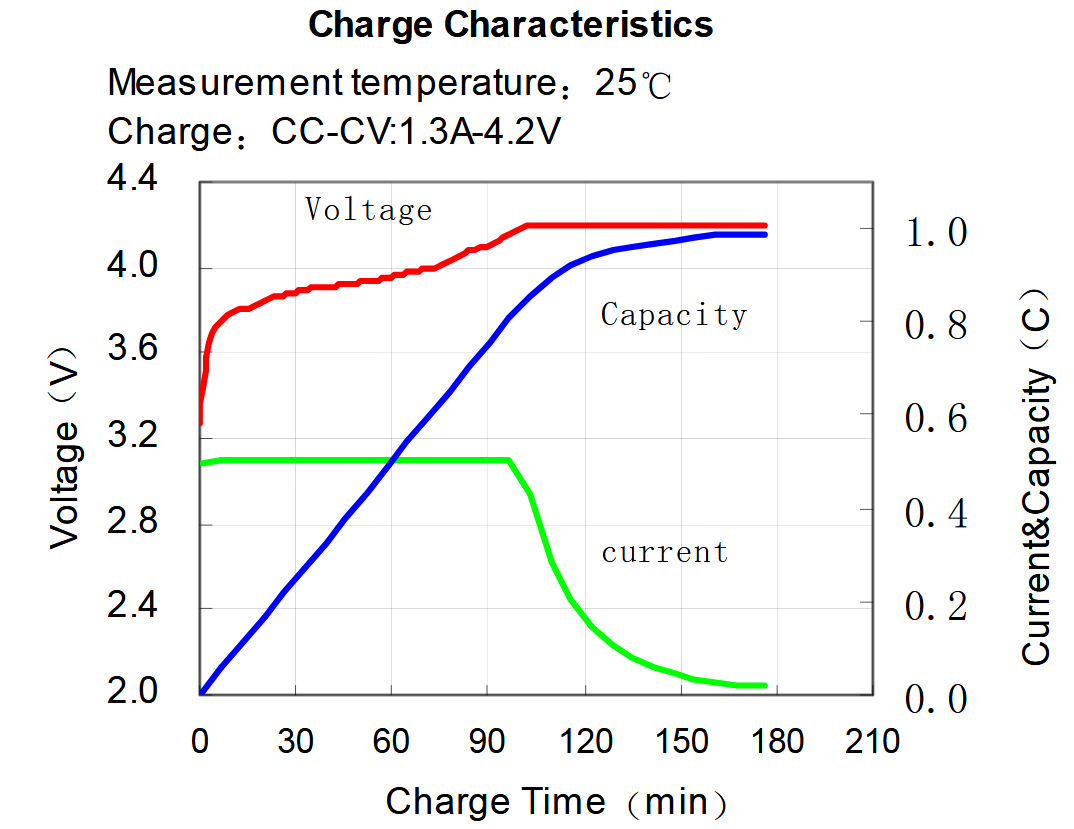
C-rate
Först lite basic om kapacitet och strömmar. Om vi har ett batteri på 1800 mAh (eller 1.8Ah), så innebär detta att det kan leverera 1800 mA (eller 1.8A) under en timme, teoretiskt. Vi kallar detta urladdningstempo 1C. Samma batteri kan lämna ifrån sig 900 mA under 2 timmar, vi kallar det urladdningstempot 0.5C. Omvänt förhåller det sig på samma sätt vid laddning. Om vi laddar ett batteri på 1800 mAh med 900 mA, så är detta ett laddningstempo på 0.5C. Det kommer dock ta lite mer än 2 timmar, då laddningströmmen sjunker mot slutet (det kommer ta 3-4 timmar). De flesta litium -batterier accepterar av säkerhetsskäl ett laddningstempo på 0.5C till 0.7C. Det finns batterier som är konstruerade så att de kan leverera både 10C och 20C under en kort period och även batterier som kan laddas snabbare men detta är undantag när det gäller litium.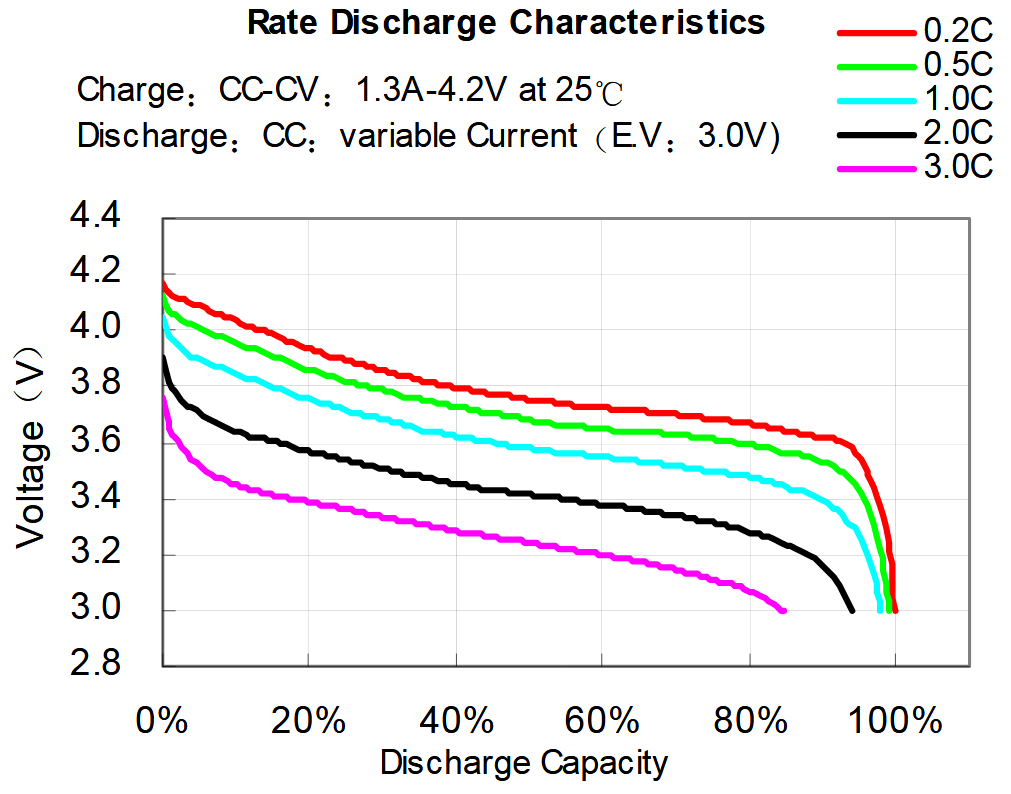
Ovan bild hur en urladdnings -karaktäristik för ett litium -batteri kan se ut. Batteriet verkar må ganska bra när det laddas ur med en hastighet under 1C. En aspekt att känna till, som iofs inte hör hit men ovan kurva påminner om, det är att en elektronisk manick som drivs av litiumbatterier måste kunna hantera att batteriets spänning sjunker längs tidsaxeln när batteriet driver någonting.
Laddning: CC/CV med auto-avstängning
Okej, tillbaka till laddningen. Det hela är inte så komplicerat, i terorin, förutsatt att man är lite noggrann och kan enkelt utföras om man har ett typiskt laboratorie-aggregat där det går att begränsa både spänningen och strömmen.Först en enkel mätning för att se att inte batterispänningen är får låg (mer om detta under överurladdning nedan). Är spänningen 3.3 volt eller högre är allt okej och man kan göra så här: Spänningen på labaggregatet skall då ställas in på cellens laddspänning vilket typiskt är 4.2 volt eller något sånt (se datablad). Sedan skall strömmen begränsas så att den aldrig är över ett visst laddvärde, vilket är typiskt 0.5C enligt ovan. En cell på 1800 mAh kan då laddas med 900 mA. Andra siffror kan vara specificerade för en viss cell, kolla datablad! Ganska enkelt alltså men extremt viktigt att varken ström eller spänning överstiger dessa värden. Om batteriet riskerar förstöras (vilket kan ske utan att det direkt märks eller att det märks väldigt väl) eller inte hänger alltså på att man är noga.

Detta innebär att litiumbatterier kan laddas enkelt med ett vanligt laboratorie-aggregat med dessa inställningar. Förutom detta kan en viss maxtid vara specificerad.
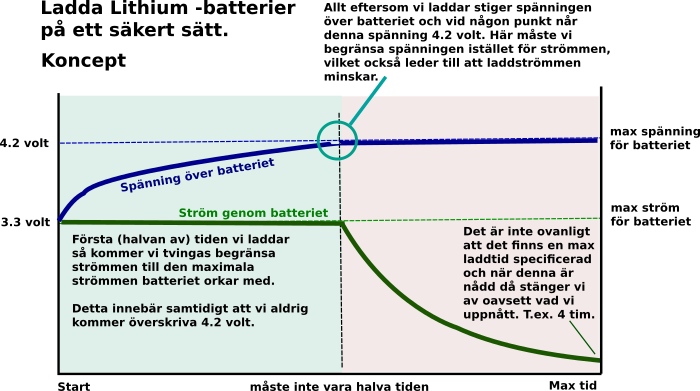
Det som kommer inträffa med ovan inställningar är att inledningsvis kommer laboratorie-aggregatet att begränsa spänningen. Spänningen kommer reduceras för att inte strömmen skall nå över max inställda ström. Som en konsekvens laddas litiumcellen med en konstant ström under en viss period och spänningen är lägre än 4.2 volt.
Allt eftersom tiden passerar stiger spänningen långsamt över cellen. Vid någon nivå slår spänningen i taket på 4.2 volt som är inställd. Här efter kommer aggregatet långsamt sänka strömmen, då det behövs allt mindre ström för att uppnå 4.2 volt. Under denna period kommer alltså spänningen ligga på denna max-spänning samtidigt som strömmen sjunker allt eftersom batteriet blir färdigladdat.
En sista grej är en tidsbegränsning, t.ex. 4 timmar, då aggregatet stänger av sig själv oavsett vad som uppnåtts. Denna tidsbegränsning har inte ett typiskt labbaggregat, så denna timer måste tillföras om man inte orkar hålla koll på det.
Ungefär detta är vad som behövs. En laddare behöver en spännings-regulator som garanterar att spänningen aldrig är över en viss nivå, t.ex. 4.2 volt, samt en strömbegränsare som också hindrar aggregatet från att lämna ifrån sig en högre ström än vad batteriet klarar. Dessa 2 funktioner bör garantera att ovanstående laddkurva upprätthålls. Ovanpå detta en timer för att stänga ner efter en viss tid oavsett vad som uppnåtts.
Lite risker med litiumbatterier
Överurladdning
Om spänningen över en cell tillåts sjunka ner mot 2 volt antingen genom att använda batteriet eller genom långvarig passiv lagring så förstörs batteriet. Om spänningen över cellen är så låg, så skall man alltså inte försöka ladda detta överhuvudtaget då batteriet troligtvis är trasigt och därför inte följer några direkta förutsägbara regler över vad som kommer hända om man försöker ladda det.Även en spänningen under 2.8-3 betraktas ibland som "överurladdat", men kan räddas genom att lägga en långsam laddcykel med låg ström (0.1C) före ovan beskrivna laddning tills dess att spänningen när 3 volt.
Det som händer vid låg spänning är att anoden löses upp i batteriets elektrolyt, vilket i sig själv ökar självurladdningen. Även katoden bryts ner, vilket kan resultera i intern kortslutning. Batteriet måste alltså laddas innan det är helt urladdat för att inte förstöras. Det finns vanligtvis en krets i batteriet som förhindrar detta från att hända som beskrivet nedan. Denna krets kommer ge sken av att batteriet är urladdat lite innan det är urladdad för att skydda batteriet. Användaren kommer därför plugga in laddaren, vilket räddar batteriet.
Överladdning
Överladdning sker typiskt om spänningen skulle överstiga 4.2 volt per cell, vilket kan hända om laddaren är trasig. Det som händer är att litium-joner inte kan fångas upp tillräckligt snabbt vilket skapar "litium-plack" på anodens yta. Flera saker kan ske p.g.a. detta. Det första är en permanent skada på batteriets kapacitet. Det andra är att det kan resultera i intern kortslutning. Ett annat problem som uppstår vid överladdning är att batteriets temperatur ökar vilket i sig skadar batteriet och kan resultera i intern kortslutning. Även detta brukar en intern krets skydda mot.För hög strömstyrka
Även detta bär en felaktig laddare skulden för. Kan leda till hög temperatur vilket kan skapa en intern kortslutning.Inbyggda skyddskretsar
För att slippa något av ovanstående problem har man hittat på att förse litium-batterier med en intern skyddskrets. Dvs, ett litet kretskort som mäter spänning och ström och som stänger av batteriet om något går fel. Det kallas Battery Management System eller BMS. Denna krets fixar också balanseringsproblemet om man i ett batteripaket seriekopplar litium-celler. Nedan ett exempel på sådan krets som kan sitta i ett litium-paket i en hoverboard. Det är alltså en hel del elektronik - i själva batteriet.

Metod 2.Använd det som följer med hoverboarden
Med den slaktade hoverboarden kom en laddare och lite annat jox. Denna laddare innehåller (borde innehålla) all elektronik nödvändig för att säkert ladda litium-batteriet i hoverboarden dvs troligtvis en CC/CV -laddare med tidsbegränsning, så denna metod är troligtvis den mest säkra. Den enda komponent som tillkommer här är en diod och en kondensator.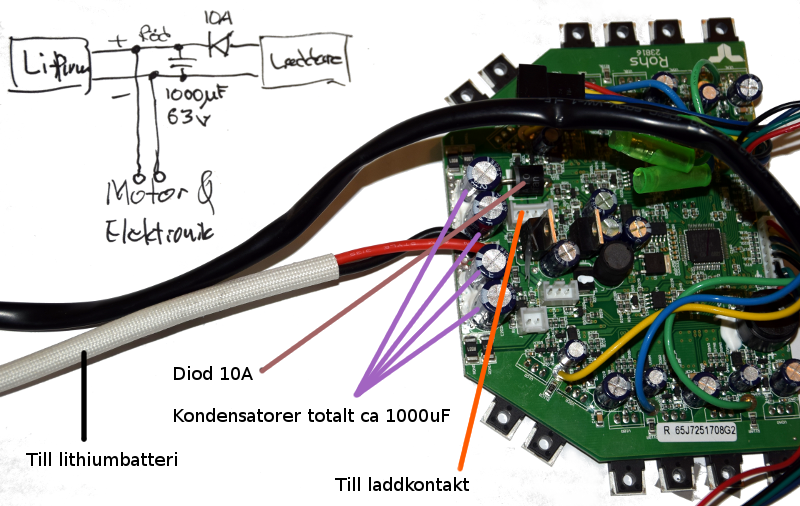
Nedan en förstoring av anslutningskontakten till laddar-uttaget på hoverboarden. Intill ser du dioden som sedan är kopplad i serie med plus till litium-batteriet. De 4 stycken parallellkopplade kondensatorerna är på tillsammans 1000 uF.


Nedan ihopsnickrat med ovan laddkontakt och XT60-kontakten för batteriet och en dioden som någon vill ska finnas där.

Intresseklubben noterar:
Blybatteriet kom år 1890 ungefär och används fortfarande till startmotorer i bilar. Energidensiteten är ca 30 Wh/kg. Ni-Cd (Nickel Kadmium) kom på 50-talet och har en energidensitet på ca 50 Wh/kg. Ni-Cd blev det vanligaste laddbara batteriet i hemelektronik fram till 90-talet då Ni-MH (Nickelmetallhydrid) tog över med energidensitet på 80 Wh/kg. Nickelmetallhydrid hade också den tilltalande egenskapen att det var relativt miljövänligt, medans bly och kadmium är farliga grundämnen för levande organismer. I princip all bly i blybatteriet återvinns och kan användas i nya blybatterier, men bly är fortfarande ett farligt ämne för alla levande organismer.På 90-talet gjorde litiumbatterierna sitt intåg, med en energidensitet på 100-265 Wh/kg beroende på variant. Denna höga energidensitet ger små lätta batterier med väldigt hög effekt jämfört med tidigare alternativ. Litium är också miljövänligt. En annan stor fördel med litiumbatterier är den låga självurladdningen ca 5% per månad mot kanske 20% för bly eller nickel (varierar stort). Litiumbatterier - jämfört med sina föregångare - är dock lite känsligare i laddprocessen.
En ofrånkomlig aspekt av att trycka in mycket hög energi på liten volym är också att litiumbatterierna generellt är farligare och kan börja brinna eller tom explodera om man har otur vid felaktig hantering. Det är på sätt och vis krass fysik. Framtida batterier med ännu högre energidensitet kommer således att potentiellt bli ännu mer farliga. Det är något vi får lära oss leva med och hantera på något sätt. Ett sätt att hantera det är att använda skyddsglasögon vid labbande!